
转自国家药品监督管理局药品审评中心
为规范研发期间安全性更新报告的撰写与管理,根据《药品注册管理办法》相关规定,药审中心组织制定了《研发期间安全性更新报告管理规范(试行)》(见附件),经国家药品监督管理局审核同意,现予发布,自2020年7月1日起施行。
原国家食品药品监督管理局药品审评中心《关于化学药IND申请药学研究数据提交事宜的通知》(2012年5月10日发布)中要求的《化学药IND申请药学研究年度报告(试行)》与研发期间安全性更新报告统一,不再单独提交。
特此通告。
研发期间安全性更新报告管理规范(试行)
第一条 为规范研发期间安全性更新报告(以下简称DSUR)的撰写与管理,根据《药品注册管理办法》相关要求,制定本管理规范。
第二条 DSUR的主要目的是药品注册申请人(以下简称申请人,也包括申办者)对报告周期内收集到的与药物(无论上市与否)相关的安全性信息进行全面深入的年度回顾和评估。
第三条 申请人应按照国际人用药品注册技术协调会(以下简称ICH)E2F《研发期间安全性更新报告》(以下简称E2F指导原则)的要求准备、撰写和提交DSUR。
申请人可以委托第三方(如合同研究组织)进行DSUR的准备、撰写和提交工作,但申请人仍对DSUR的内容、质量和提交时间承担主体责任。对于共同开发等涉及多方情况的,申请人应按ICH E2F指导原则“各方的责任”一节对DSUR准备与提交的责任进行划分。
第四条 申请人在准备DSUR时,需要包含与所有剂型和规格、所有适应症以及研究中接受研究药物的患者人群相关的数据(化学药和生物制品应按照相同活性成分,中药按照相同处方进行准备)。如果相关信息无法获得(如申请人尚未获得数据),申请人应在DSUR的前言部分予以解释说明。
第五条 申请人获准开展药物 (包括中药、化学药及生物制品 )临床试验后均应向国家药品监督管理局药品审评中心(以下简称药品审评中心)提交DSUR。
第六条 DSUR原则上应将药物临床试验在境内或者全球首次获得临床试验许可日期(即“国际研发诞生日”,以下简称DIBD)的月和日,作为年度报告周期的起始日期。首次提交应在境内临床试验获准开展后第一个DIBD后两个月内完成,后续提交也应以DIBD为基准。
第七条 DSUR应持续提交至该药物境内最后一个上市许可申请提交,或者在境内不再继续进行研发时为止。最后一次提交时应附说明文件,说明该次提交为在境内的最后一份DSUR,并说明申请人是否还在其他国家或者地区继续进行临床试验。
第八条 当药物在境内外获得了上市许可,如申请人需要,可以在全球首个获得上市批准日期(即“国际诞生日”,以下简称IBD)的基础上准备和提交DSUR。调整后的首次提交,报告周期不应超过一年。
第九条 申请人在提交DSUR时,应包括以下文件:
1. DSUR全文及附件;
2. 报告周期内申请人认为不影响受试者安全的药物临床试验方案变更或者临床方面的新发现、非临床或者药学的变化或者新发现的支持性资料。
申请人还应视情况(如最后一次提交DSUR),随DSUR提交必要的说明性文件。
第十条 申请人应严格按照ICH E2F指导原则要求,逐章节完整撰写DSUR及附件。对于无进展/无发现的章节或者附件,应在相应项下进行说明,不可省略。
申请人在组织撰写DSUR时,应在“区域特有信息”一节中,将报告周期内,结合相关法规、技术指南等要求,对发生的药物临床试验方案变更或者临床方面的新发现、非临床或者药学的变化或者新发现是否可能增加受试者安全性风险的评估结果及申报情况进行总结,并提交支持性资料。DSUR不应作为新的重要安全性信息的初始报告途径,或者新的安全性问题的检出途径。
第十一条 DSUR采用中文进行报告,对于“报告周期内严重不良反应行列表”可采用中文或者英文报告。
第十二条 申请人在撰写DSUR时,需在“区域特有信息”项下或者以DSUR区域附件形式提供以下信息:
1.严重不良反应(SAR)累计汇总表;
2.报告周期内境内死亡受试者列表;
3.报告周期内境内因任何不良事件而退出临床试验的受试者列表;
4.报告周期内发生的药物临床试验方案变更或者临床方面的新发现、非临床或者药学的变化或者新发现总结表;
5.下一报告周期内总体研究计划概要。
详细撰写要求参见附件1至附件5和附表。
第十三条 申请人可通过药品审评中心网站等规定的途径提交DSUR。经审核,认为需提醒或要求申请人的(如,要求申请人更改DSUR报告周期、补充更正资料或者提醒申请人应加强受试者安全性措施等),药品审评中心将在DSUR提交后一百八十个工作日内通知申请人。申请人应通过药品审评中心网站查询和下载相关通知或者提醒,对于需要补充更正资料的情况,申请人应在收到补正意见之日起的五个工作日内一次性提交补正资料。
第十四条 本管理规范自2020年7月1日起施行。
1.严重不良反应(SAR)累计汇总
2.报告周期内死亡受试者列表
3.报告周期内境内因任何不良事件而退出临床试验的受试者列表
4. 报告周期内发生的药物临床试验方案变更或者临床方面的新发现、非临床或者药学的变化或者新发现总结表
5. 下一报告周期内总体研究计划概要
SAR累计汇总表中应指明自DIBD起全部SAR的数量,需按照下列方式分类:
1.系统器官分类(SOC);
2.不良反应术语;
3.治疗组(如适用)。
同时,应对非预期的不良反应术语加以标注。
申请人应参照《E2F DSUR 示例 商业申办者》附录R1进行编写。
临床试验过程中境内死亡受试者列表应至少包括:受试者编号、治疗方案(可能仍处于盲态)以及每例受试者死亡的原因。若在对受试者死亡进行的评估中发现任何安全性问题,应根据具体情况在DSUR第18节“整体安全性评估”中进行说明。
申请人可参照《E2F DSUR 示例 商业申办者》附录R2进行编写。若使用该格式,请在“试验编号”项下同时填写该临床试验在“药物临床试验登记与信息公示平台”中的“登记号”(如CTR20XXXXXX)。
附件3
报告周期内境内因任何不良事件而退出临床试验的受试者列表
该列表应包括报告周期内境内因任何不良事件而退出临床试验的所有受试者,无论是否与药物相关。若在对受试者退出的评估中发现了任何安全性问题,应根据具体情况在DSUR第18节“整体安全性评估”中进行说明。
申请人可参照《E2F DSUR 示例 商业申办者》附录R3进行编写。若使用该格式,请在“试验编号”项下同时填写该临床试验在“药物临床试验登记与信息公示平台”中的“登记号”(如,CTR20XXXXXX)。
附件4
报告周期内发生的药物临床试验方案变更或者临床方面的新发现、非临床或者药学的变化或者新发现总结表
申请人应以列表形式,对报告周期内发生的药物临床试验方案变更、非临床或者药学的变化或者新发现进行总结,示例参见附表1。
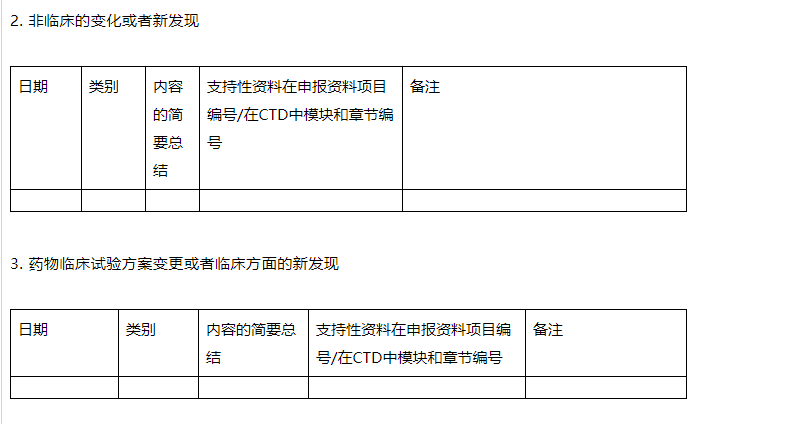
对于可能增加受试者安全性风险的,申请人应按照药学的变化或者新发现、非临床的变化或者新发现、药物临床试验方案变更或者临床方面的新发现三种类别,总结已提交的补充申请的受理号、申请事项、承办日期及是否获批(是/否/在审)。不需提供支持性资料。
对于申请人评估认为不影响受试者安全的,申请人应按照药学的变化或者新发现、非临床的变化或者新发现、药物临床试验方案变更或者临床方面的新发现三种类别,总结其内容、时间、类别,并注明对应支持性资料的申报资料项目编号或者人用药物注册申请通用技术文档(以下简称CTD)中的模块及章节编号。申请人应参照化学药、生物制品和中药注册分类及申报资料要求、CTD等要求,准备相应的支持性资料与DSUR一并提交。对于报告周期内已提交过的相关资料(如用于沟通交流的资料,因开展后续分期药物临床试验,已在药品审评中心网站提交的药物临床试验方案和支持性资料),应在备注栏中注明提交途径、时间和参考编号(如沟通交流申请编号等),不需重复提交。
报告周期内发生的药物临床试验方案变更或者临床方面的新发现、非临床或者药学的变化或者新发现总结表

下一报告周期内总体研究计划概要
申请人应简要提供以下内容:
一、下一报告周期内临床研究总体计划概要
(一)立题依据;
申请人应简要描述下一报告周期内计划进行的临床试验的立题依据。
(二)拟研究的适应症;
申请人应列出下一报告周期内,计划进行研究的未上市适应症。
(三)评价药物时所遵循的总体路径;
简要描述下一报告周期内,计划开展临床试验的顺序或者对计划研究的患者人群进行简要描述。
(四)下一个报告周期内拟开展的临床试验;
简要描述下一报告周期内,计划开展的临床试验的试验设计(如果没有制定全年的计划,申请人应予以注明)。
(五)预计受试者人数;
下一报告周期内计划开展的临床试验中,估计的受试者人数;
(六)预计的风险。
基于动物的毒理学或者既往人用试验的数据,预计的任何与药物或者相关药物有关的严重或者重度风险。
二、下一报告周期内非临床研究总体计划概要
简要描述下一报告周期内计划新开展或者继续进行的非临床研究。
三、下一报告周期内药学研究总体计划概要
简要描述下一报告周期内计划新开展或者继续进行的药学研究。
版权声明
本文部分内容转自"国家药品监督管理局药品评审中心"官网,所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(info@simoonrecordcom),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场。

